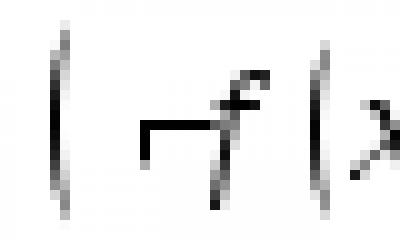Или замещением уходящей группы,
напр. нуклеоф. замещение у насыщ. атома углерода или в ароматич. кольце, нуклеоф.
присоединение к карбонильной группе или алкенам и алкинам , нуклеоф. замещение
у карбонильного атома углерода , нуклеоф. замещение у атома фосфора .
Наиб. изучены р-ции н у
к л е о ф. з а м е щ е н и я у н а с ы щ. а т о м а у г л е р о д а:
Р-ции такого типа обычно
используют также для качеств. и количеств. определения понятий, характеризующих
нуклеофильные реакции .
В этих р-циях нуклеофилом
является частица X:, предоставляющая орг. субстрату пару электронов . Для уходящей
со своей парой электронов группы Z: принято назв. н у к л е о-ф у г (от лат.
nucleus-ядро и fugio-убегаю). На скорость и механизм р-ции нуклеоф. замещения
определяющее влияние оказывают нуклеоф. реакц. способность (или нуклеофиль
ность,
"нуклеофильная сила") реагента X:, нуклеофугная рсакц. способность
(или нуклеофугность) уходящей группы Z:, природа субстрата и условия р-ции (т-ра,
р-ритель, давление и т. д.). Нуклеофильность, в отличие от основности, является
величиной кинетической, а не термодинамической, т. е. количеств. мерой нуклеоф.
реакц. способности служит константа скорости р-ции, а не константа равновесия .
Различают два предельных
случая р-ций нуклеоф. замещения-мономол. процесс S N 1 и
бимолекулярный (синхронный) S N 2:

Механизм нуклеоф. замещения
существенно зависит от природы субстрата и р-рителя. Так, процессы S N 1
реализуются в полярных р-рителях (Н 2 О, СН 3 ОН, АсОН
и др.), способствующих гетеролизу связи С-Z, и в р-циях с субстратами , содержащими
третичный, аллильный или бен-зильный атом С. Процессы S N 2
в меньшей степени зависят от р-рителя и наиб. характерны для субстратов
с первичным атомом С.
При мономол. процессе первоначально
под действием р-рителя происходит ионизация субстрата с образованием трехкоординац.
карбкатиона и нуклеофуга (эта стадия обычно определяет скорость всего процесса),
а затем следует быстрая стадия связывания карбкатиона с нуклеофилом. При этом
атака нуклеофила равновероятна с обеих сторон, и в случае асимметрич. реакц.
центра обычно наблюдается образование рацематов . При бимол. процессе образуется
пятикоординац. переходное состояние, причем атака нуклеофила осуществляется
со стороны, противоположной уходящему заместителю, что приводит к обращению
конфигурации, напр. т. наз. вальденовское обращение (см. Динамическая стереохимия).
Р-ция S N l
обычно имеет суммарный 1-й порядок; скорость ее, как правило, не зависит
от природы нуклеофила и его концентрации , но сильно зависит от природы нуклеофуга
и р-рителя. Кинетика р-ции S N 2 описывается ур-нием
2-го порядка - первого по субстрату и первого по нуклеофилу. Скорость р-ции
в этом случае зависит как от концентрации , так и от хим. природы нуклеофила.
Известно неск. подходов
к количеств. оценке нуклеоф. реакц. способности реагента X: на основе корреляц.
соотношений как в S N 2-, так и S N 1-процессах.
Для р-ций S N 2 в воде или метаноле наиб. широко применяют
ур-ние Свена-Скотта lg (k/k 0) = S . n,
где k и k 0 -константы скорости р-ции субстрата соотв.
с данным нуклеофилом и водой , S- параметр чувствительности субстрата
к изменению нуклеофила (S = 1 для стандартного субстрата-СН 3 Вr),
и-параметр нуклеофильности реагента (табл. 1).
Табл.
1.-ЗНАЧЕНИЕ
ПАРАМЕТРА НУКЛЕОФИЛЬНОСТИ п ДЛЯ НЕКОТОРЫХ РЕАГЕНТОВ (вода , 25 °С)

Для процессов типа S N l
справедливо корреляц. ур-ние Ритчи lg(k/k 0) = N + .
Оно получено измерением скоростей р-ций с использованием в качестве субстратов
карбкатио-нов, стабилизированных арилъными заместителями три-фенилметанового
ряда.
Параметр нуклеофильности
N + характеризует реакц. способность нуклеофила в определенном р-рителе;
в воде величины N + близки к параметрам п.
Величины параметров нуклеофильности
могут заметно меняться в зависимости от конкретной нуклеофильной реакции , однако общая тенденция
изменения нуклеофильности обычно сохраняется. Так, практически во всех нуклеофильных реакциях
ОН - , CN - , RS - , I - и Вr - проявляют
себя как сильные нуклеофилы, а Н 2 О, СН 3 ОН, F - ,
NO - 3 , SО 4 2- -как слабые.
Мерой нуклеофугности могут
служить константы скорости сольволиза (протекающего по механизму S N 1)
однотипных субстратов , отличающихся лишь природой уходящей группы (табл.
2).
Табл.
2. ОТНОСИТЕЛЬНЫЕ
КОНСТАНТЫ СКОРОСТИ СОЛЬВОЛИЗА
(k отн)
НЕКОТОРЫХ УХОДЯЩИХ ГРУПП [субстрат-Ph(CH 3)CHZ в 80%-ном
водном
этаноле , 75°С]

К "хорошим"
нуклеофугам относят орг. сульфонат-(този-лат, мезилат, трифлат), фторсульфат-(FSО - 3)
и перхлорат-анионы(СlO - 4). Ковалентные орг. производные
этих анионов широко используют в качестве алкилирующих реагентов-чрезвычайно
активных субстратов в нуклеофильных реакциях . Еще более хорошие нуклеофугные частицы-азот из алкилдиазониевых
солей (RN + 2), трехвалентный иод (напр., группа IСl 2),
вода из
протонир.
спирта
и простой эфир из триалкилоксо
ниевых
солей ;
однако алифатич. субстраты , содержащие в своей структуре эти группы, при комнатной
т-ре обычно неустойчивы и используются лишь в качестве активных интермедиатов ,
генерируемых непосредственно в реакц. среде.
Существует неск. разл.
подходов к теоретич. интерпретации понятий нуклеофильности и нуклеофугности
и к оценке факторов, влияющих на их величину. Осн. факторы - основность (кислотность),
поляризуемость , сольватац. эффекты, величины потенциалов ионизации и окисления ,
стерич. и электростатич. эффекты, наличие своб. электронной пары у атома , соседнего
с нуклеоф. центром, прочность связи с атомом углерода . Следует отметить, что
прямой корреляции нуклеофильности с к.-л. одним из этих параметров обычно нет,
как нет и корреляции между нуклеофильностью и нуклеофугностью; напр., тиолят-анион
RS - -хороший нуклеофил, но слабое основание и "плохая"
уходящая группа, гидроксид-анион НО - -хорошее основание и нуклеофил,
но плохая уходящая группа. Анионы самых сильных к-т-хлорной и трифторметансульфоновой
- хорошие нуклеофу-ги и в то же время способны проявлять нуклеофильные свойства.
Нуклеоф. замещение в алифатич.
ряду имеет исключительно важное значение для орг. синтеза, позволяя целенаправленно
заменять функц. группы, а также конструировать углеродный скелет молекулы путем
использования С-нуклеофилов (напр., металлоорг. соединений).
Н у к л е о ф. з а м е
щ е н и е в а р о м а т и ч. р я д у (ароматич. нуклеоф. замещение) обычно сильно
затруднено и может протекать по механизмам "присоединение - отщепление"
или через промежут.
образование дегидробензола (арино-вьш механизм):

В первом случае первоначально происходит присоединение нуклеофила к ароматич. субстрату с образованием промежут. продукта (иногда стабильного - т. наз. комплекс Майзенхаймера), отщепление нуклсофуга от к-рого приводит к конечному продукту замещения. Электроноакцеп-торные заместители в ядре (NO 2 , COR, CN и др.) стабилизируют
Нуклеофильные реакции – гетеролитические реакции органических соединений с нуклеофильными реагентами. К нуклеофилам относятся анионы и молекулы (органические и неорганические), которые в ходе реакции расходуют свою неподеленную пару электронов на образование новой связи.
На скорость и механизм реакции S N определяющее влияние оказывают:
Нуклеофильная способность (нуклеофильность) реагента Y
Природа субстрата
Нуклеофугная способность уходящей группы
Условия реакции
Нуклеофильность, в отличии от основности, величина кинетическая, а не термодинамическая, т.е. количественной мерой нуклеофильности является константа скорости реакции, а не константа равновесия.
Есть 2 предельных случая S N:

Sn. Квантово-химические представления
![]()
S N можно представить как взаимодействие ВЗМО нуклеофила и НСМО субстрата. Энергия взаимодействия:
![]()
,– заряды на реакционном центре нуклеофила Y и атоме углерода субстрата, по которому осуществляется атака.
– расстояние между реагирующими центрами.
– коэффициент атомной орбитали атома, принадлежащего нуклеофилу, который является нуклеофильным центром, т.е. характеризует вклад атома нуклеофила в ВЗМО Y.
– характеризует вклад атома углерода (электрофильный центр) в НСМО субстрата.
– изменение резонансного интеграла, характеризующий эффективность перекрывания ВЗМО Y и НСМО субстрата.
,– энергии ВЗМО Y и НСМО субстрата.
В случае S N 1, когда осуществляется взаимодействие катиона и аниона и реакционный центр несет положительный заряд, определяющая – кулоновская составляющая и относительная реакционная способность нуклеофилов увеличиваться симбатно их основности. В этом случае говорят, что реакция идет при зарядовом контроле.
Более сложная ситуация в S N 2. В газовой фазе и апротонных растворителях, где сольватация аниона мала и заряд на нуклеофиле в большей степени локализован, также наблюдается зарядовый контроль. Однако в протонных растворителях (спирты) заряд на нуклеофиле делокализован в результате сольватации. Заряд на реакционном центре также мал. В этом случае роль кулоновского взаимодействия ниже и основной вклад в энергию взаимодействия вносит орбитальная составляющая. Говорят, что реакция идет при орбитальном контроле. Присутствие донора в нуклеофиле увеличивает заряд на реакционном центре, тем самым увеличивается вклад зарядовой составляющей, кроме того введение донорного заместителя приводит к некоторому увеличению энергии ВЗМО нуклеофила и, следовательно, к увеличению орбитальной составляющей. Т.о. введение ЭД в молекулу нуклеофила приводит к увеличению скорости реакции. В ряду галогенов как нуклеофилов кулоновское взаимодействие уменьшается от фтора к йоду, что является следствием уменьшения локализации отрицательного заряда и увеличении расстояния между атомами. В то же время орбитальное взаимодействие увеличивается, т.к. повышается энергия НСМО галогенов (ВЗМО).
В отличии от S Е, где замещению обычно подвергается атом водорода, в S N замещаются функциональные группы (галогены, сульфо-, нитро- и т.д.).
Общая схема реакции:
R - НаI + :N - → R - N + :НаI -
Нуклеофил отдает субстрату свою пару электронов, за счет которой образуется новая связь, а галоген уходит со своей парой электронов в виде галогенид-аниона. При этом происходит алкилирование нуклеофила.
Для нуклеофильного замещения у атома углерода в состоянии sp 3 -гибридизации установлено два основных механизма: бимолекулярное нуклеофильное замещение (S N 2 ) и мономолекуляное нуклеофильное замещение (S N 1 ).
Бимолекулярное нуклеофильное замещение – это синхронный процесс, который протекает в одну стадию. Разрыв старой и образование новой связи происходят одновременно. Нуклеофил атакует субстрат со стороны, противоположной уходящей группе (с тыла), и постепенно вытесняет ее из молекулы:
N: + R-Hal → → N-R + Hal -
переходное
состояние
S N 2-реакции имеют следующие основные признаки:
- Кинетический
Скорость реакции зависит от концентрации и субстрата, и нуклеофила. Реакция имеет второй общий порядок (первый по субстрату и первый по нуклеофилу) и описывается кинетическим уравнением:
2. Стереохимический
Если нуклеофильное замещение происходит у асимметрического атома углерода, то имеет место обращение конфигурации, так как в переходном состоянии три нереагирующие группы и центральный атом углерода находятся в одной плоскости, а входящая и уходящая группы расположены на одной прямой, перпендикулярной этой плоскости. В результате структура выворачивается, как зонтик.
Мономолекулярное нуклеофильное замещение протекает в две стадии.
На первой стадии под действием растворителя происходит гетеролитический разрыв связи в субстрате, в результате чего образуется карбокатион. Процесс протекает медленно и определяет скорость реакции в целом. На второй стадии карбокатион быстро реагирует с нуклеофилом, давая продукт замещения.
S N 1-реакции имеют следующие основные признаки.
1. Кинетический
Скорость реакции зависит только от концентрации субстрата, поскольку нуклеофил не участвует в лимитирующей стадии процесса. Реакция имеет первый порядок и описывается кинетическим уравнением:
2. Cтереохимический признак
Если нуклеофильное замещение происходит у асимметрического атома углерода, то, как правило, образуется рацемическая смесь, так как атака нуклеофилом плоского карбокатиона с обоих сторон равновероятна.
Факторы, влияющие на ход нуклеофильного замещения
Легкость протекания реакции и ее механизм зависят от многих факторов, среди которых можно выделить следующие:
- строение углеводородного радикала субстрата;
- природа уходящей группы;
- сила нуклеофила;
- природа растворителя.
Влияние строения углеводородного радикала.
Реакционная способность первичных, вторичных и третичных алкилгалогенидов в реакциях нуклеофильного замещения различна, причем порядок реакционной способности зависит от механизма реакции.
Скорость реакций, протекающих по механизму S N 1, зависит от стабильности карбокатиона, образующегося на первой стадии реакции. Таким образом, реакционная способность алкилгалогенидов в реакциях S N 1 возрастает в ряду: перв <вторич< третич
который соответствует ряду стабильности карбокатионов.
Успех реакции S N 2 определяется эффективностью атаки нуклеофила на положительно заряженный реакционный центр субстрата. Поэтому электронодонорные радикалы R, понижая положительный заряд на реакционном центре, замедляют нуклеофильную атаку. Увеличение объема R затрудняет подход нуклеофила к реакционному центру. Совместное действие индуктивного и объемного эффектов определяет ряд реакционных особностей субстратов в реакциях нуклеофильного замещения: перв >вторич> третич.
Высокой реакционной способностью, независимо от механизма реакции, обладают аллил- и бензилгалогениды. В процессе S N 1 они образуют карбокатионы, стабилизированные засчет р, π-сопряжения:
Легкость, с которой аллил- и бензилгалогениды вступают в S N 2-реакции, объясняют участием кратных связей в стабилизации переходного состояния.
Влияние природы уходящей группы.
Реакционная способность алкилгалоненидов зависит от прочности связи углерод – галоген, которая уменьшается в ряду:
C-F > C-Cl > C-Br > C-I.
Не менее важно, чтобы уходящая группа была термодинамически стабильна. (Она должна быть более устойчива, чем атакующий субстрат нуклеофил). Хорошими (относительно устойчивыми) уходящими группами являются слабые основания. Галогенид-анионы – хорошие уходящие группы. Относительная стабильность возрастает по мере уменьшения их основности в ряду:
F - < Cl - < Br - < I -
Параллельно увеличивается и реакционная способность алкилгалогенидов:
RF < RCl < RBr < RI
Влияние природы нуклеофила.
Нулеофильность – это способность частицы взаимодействовать с атомом углерода, несущим целый или частичный положительный заряд. Нуклеофильность является кинетической характеристикой и определяется константами скоростей соответствующих реакций.
Нуклеофилы, как и основания, могут быть сильными и слабыми. Единой шкалы нуклеофильности не существует, так как относительная сила нуклеофила может изменяться в зависимости от природы субстрата и растворителя. Однако можно выделить следующие основные закономерности:
1) отрицательно заряженные нуклеофилы сильнее, чем нейтральные молекулы (сопряженные им кислоты):
OH - > H 2 O; RO - > ROH; NH 2 - > NH 3
2) для элементов одного периода с ростом электроотрицательности атома нуклеофильность уменьшается:
NH 2 - > OH - > F -
R 3 C - > RNH 2 - > RO - > F -
3) электронодонорные заместители увеличивают, электроноакцепторные – уменьшают нуклеофильность. Например, для кислородсодержащих нуклеофилов установлен следующий ряд реакционной способности:
RO - > OH - > ArO - > RCOO -
В рассмотренных примерах порядок нуклеофильности реагентов совпадает с порядком их основности и объясняется теми же причинами. Однако сила нуклеофила определяется не только его основностью, но и поляризуемостью .
4) Для элементов одной подгруппы с возрастанием заряда ядра нуклеофильность увеличивается, несмотря на уменьшение основности:
I- > Вr- > Cl- > F-
Рост нуклеофильности связан с увеличением поляризуемости атомов и ионов по мере увеличения их радиуса. Чем выше поляризуемость нуклеофила, тем легче деформируется его электронное облако и тем в большей степени он способен передать электронную плотность субстрату.
Такой порядок нуклеофильности может быть объяснен также с позиций принципа ЖМКО. Основность по Бренстеду проявляется во взаимодействии с жесткой кислотой Н+, в то время как нуклеофильность проявляется во взаимодействии с более мягким кислотным центром – атомом углерода, для которого предпочтительным будет взаимодействие с мягкими основаниями Льюиса – RS- и I-.
Относительная сила нуклеофилов зависит от природы растворителя. Чем меньше размер аниона, тем лучше он сольватируется полярными протонными растворителями (т.е. растворителями, способными образовывать с анионом водородные связи), что снижает его реакционную способность. При замене растворителя порядок реакционной способности нуклеофилов может меняться на противоположный.
В соответствии с механизмами S N 2 и S N 1 природа нуклеофила оказывает влияние на ход S N 2-реакции, так как нуклеофил участвует в лимитирующей (и единственной) стадии процесса, и не влияет на скорость реакций, протекающих по механизму S N 1, лимитирующая стадия которых протекает без участия нуклеофила.
Влияние природы растворителя
Растворитель влияет на скорость и механизм реакций нуклеофильного замещения.
Протеканию реакции по механизму S N 1 способствуют сильноионизирующие растворители. К ним относятся полярные протонные растворители (вода, спирты, карбоновые кислоты), так как они хорошо сольватируют ионные интермедиаты: отрицательно заряженную уходящую группу – за счет водородных связей, карбокатион – за счет свободных пар электронов.
Влияние растворителя на SN2-реакции проявляется в меньшей степени и зависит от распределения зарядов в исходном и переходном состояниях. Как правило, их скорость уменьшается с ростом полярности растворителя и увеличивается при переходе от протонных растворителей к апротонным (диметилформамид, диметилсульфоксид, ацетонитрил). В апротонных растворителях, которые не способны к образованию водородных связей, нуклеофил (а это, как правило, анион) в меньшей степени сольватирован и, следовательно, обладает большей силой, что важно для S N 2-реакции.
Таким образом, протеканию реакций по механизму S N 2 способствуют:
- субстрат с углеводородным радикалом малого объема (первичным);
- апротонный растворитель;
- сильный нуклеофил.
Реализации механизма S N 1 способствуют:
- субстрат с углеводородным радикалом разветвленного строения (третичным);
- полярный протонный растворитель;
- слабый нуклеофил.
По легкости замещения галогена независимо от механизма реакции галогенпроизводные располагаются в следующий ряд:
аллил- и бензилгалогениды > алкилгалогениды > винил- и арилгалогениды
Галогенпроизводные, содержащие связь (винил- и арилгалогениды), обладают очень низкой реакционной способностью. Реакция протекает по иному механизму. Малую подвижность галогена в винил- и арилгалогенидах объясняют увеличением прочности связи C-Hal за счет сопряжения пары электронов галогена с электронами π -связей:
Реакции нуклеофильного замещения галогена широко используются в органическом синтезе. С их помощью можно заменять галоген на другие функциональные группы или углеводородные радикалы и получать из галогенпроизводных любые классы органических соединений.
Примеры синтетического использования галогенпроизводных алифатических углеводородов приведены в таблице.
Таблица. S N -реакции галогенпроизводных
| Субстрат | + | нуклефил | → | продукт + уходящая группа |
| Получение спиртов | ||||
| R-Hal | + | OH - (H 2 O) | → | R-OH + Hal - (HHal) |
| CH 3 Br | + | NaOH | CH 3 OH + NaBr | |
| (CH 3) 3 CCl | + | H 2 O | → | (CH 3) 3 COH + HCl |
| CH 2 =CH-CH 2 Cl | + | H 2 O | → | CH 2 =CHCH 2 OH+HCl |
| Получение простых эфиров | ||||
| R-Hal | + | R / O - | → | R-OR / + Hal - |
| СH 3 I | + | CH 3 CH 2 O - Na + | → | CH 3 OCH 2 CH 3 + NaI |
| Получение сложных эфиров | ||||
| R-Hal | + | R / COO - | → | R / COOR + Hal - |
| CH 3 CH 2 I | + | CH 3 COO - Na + | → | CH 3 COOCH 2 CH 3 + NaI |
| Получение тиолов | ||||
| R-Hal | + | SH - | → | R-SH + Hal - |
| CH 3 СH 2 Br | + | NaHS | → | CH 3 СH 2 SH + NaBr |
| Получение сульфидов | ||||
| R-Hal | + | R / S - | → | R-SR / + Hal - |
| CH 3 СH 2 Br | CH 3 СH 2 S - Na + | → | (CH 3 СH 2) 2 S + NaBr | |
| Получение аминов и аммониевых солей | ||||
| R-Hal | + | NH 2 - | → | RNH 2 + Hal - |
| R-Hal | + | R / 3 N | → | R R / 3 N + Hal - |
| Получение нитрилов | ||||
| R-Hal | + | С N - | → | R- С N + Hal - (S N 2) |
| CH 3 СH 2 Br | + | NaCN | → | CH 3 СH 2 CN + NaBr |
| Получение нитросоединений | ||||
| R-Hal | NO 2 - | → | R-NO 2 + Hal - (S N 2) | |
| CH 3 CH 2 I | AgNO 2 | → | CH 3 CH 2 NO 2 + AgI | |
| Получение галогенпроизводных | ||||
| R-Hal | + | I - | → | R-I + Hal - (S N 2) |
| CH 3 Cl | + | NaI | → | СH 3 I + NaCl |
Винил- и арилгалогениды инертны по отношению к нуклеофильным реагентам. Замещение галогена в галогенбензолах возможно только в очень жестких условиях.
Введение электроноакцепторных заместителей в орто - и пара -положения к галогену активизируют галогенарены в S N -реакциях.
Реакции элиминирования
В процессе отщепления (дегидрогалогенирования) от молекулы галогеноводорода отщепляется HHal и образуется алкен.
Отщепление протекает под действием сильных оснований – концентрированных растворов гидроксидов щелочных металлов в спирте, алкоголятов или амидов щелочных металлов. Основания отщепляют протон в ß -положении, одновременно из молекулы уходит галоген в виде галогенид-аниона.
Если возможно образование двух разных продуктов отщепления, то преимущественно образуется наиболее замещенный у двойной связи алкен, который является термодинамически более стабильным (правило Зайцева) :
Реакции элиминирования могут протекать, по мономолекулярному (Е1) или бимолекулярному (Е2) механизмам.
Е1-реакции протекают параллельно с реакциями S N 1 и включают две стадии. Сначала образуется карбокатион, от которого затем отщепляется под действием основания протон.
Реакции Е2 протекают параллельно с реакциями S N 2 и включают одну стадию, в ходе которой одновременно происходит разрыв старых и образование новых связей.
Механизм отщепления (Е1 или Е2) определяется теми же факторами, что и соответствующие процессы нуклеофильного замещения (SN1 и SN2).
Конкуренция реакций нуклеофильного замещения и элиминирования
Процессы отщепления и нуклеофильного замещения всегда протекают параллельно, так как все нуклеофилы одновременно являются и основаниями.
Соотношение продуктов отщепления и замещения зависит от природы реагентов и условий проведения реакции. Подбирая условия реакции и реагент, можно добиться преимущественного протекания реакции в нужном направлении.
Факторы, способствующие протеканию отщепления:
1) Высокая основность реагента.
Сильные основания будут атаковать в первую очередь атом водорода в ß -положении, а не углерод. Так, под действием алкоголят-анионов, которые являются сильными основаниями, протекает в основном отщепление, в то время как менее основные тиолят-анионы реагируют по атому углерода и дают продукты замещения:
CH 3 -CHI-CH 3 + C 2 H 5 O - Na + → CH 3 -CH=CH 2 + C 2 H 5 OH + NaI
CH 3 -CHI-CH 3 + C 2 H 5 S - Na + → (CH 3) 2 CH-S-C 2 H 5 +NaI
Протеканию отщепления способствует не только высокая основность, но и большой объем реагента, что затрудняет его атаку по атому углерода. Поэтому третичные алкоголят-анионы дают, основном, продукты отщепления.
2) Малополярные растворители.
Один и тот же реагент – гидроксид калия, в водном растворе реагирует как нуклеофил с образованием продуктов замещения, а в менее полярном растворителе – спирте дает в основном продукты отщепления.
3) Высокая температура.
Реакции отщепления имеют большую энергию активации, чем реакции замещения, и поэтому их скорость возрастает в большей степени при увеличении температуры.
4) Протеканию отщепления способствует большой объем углеводородного радикала субстрата, что затрудняет атаку реагента по атому углерода. Склонность галогенпроизводных к реакциям отщепления возрастает в ряду:
первичные < вторичные < третичные
Взаимодействие оснований с третичные алкилгалогениды приводит в основном к отщеплению.
Лекция № 11
АЛЬДЕГИДЫ И КЕТОНЫ
Альдегиды и кетоны содержат карбонильную группу С=О. Общая формула:
Методы получения.


Химические свойства.
Альдегиды и кетоны – один из наиболее реакционноспособных классов органических соединений. Их химические свойства определяются присутствием карбонильной группы. Вследствие большого различия в электроотрицательностях углерода и кислорода и высокой поляризуемости π -связи связь С=О обладает значительной полярностью (µ С=О =2,5-2,8 D). Атом углерода карбонильной группы несет эффективный положительный заряд и является объектом для атаки нуклеофилов. Основной тип реакций альдегидов и кетонов – реакции нуклеофильного присоединения A N . Кроме того, карбонильная группа оказывает влияние на реакционную способность связи С-Н в α -положении, повышая ее кислотность.
Таким образом, молекулы альдегидов и кетонов содержат два основных реакционных центра – связь С=О и связь С-Н в α -положении:

2.1. Реакции нуклеофильного присоединения.
Альдегиды и кетоны легко присоединяют нуклеофильные реагенты по С=О связи. Процесс начинается с атаки нуклеофила по карбонильному атому углерода. Затем образующийся на первой стадии тетраэдрический интермедиат присоединяет протон и дает продукт присоединения:

Активность карбонильных соединений в A N –реакциях зависит от величины эффективного положительного заряда на карбонильном атоме углерода и объема заместителей у карбонильной группы. Электронодонорные и объемистые заместители затрудняют реакцию, электроноакцепторные заместители повышают реакционную способность карбонильного соединения. Поэтому альдегиды в A N –реакциях активнее, чем кетоны:
Активность карбонильных соединений повышается в присутствии кислотных катализаторов, которые увеличивают положительный заряд на карбонильном атоме углерода:

Альдегиды и кетоны присоединяют воду, спирты, тиолы, синильную кислоту, гидросульфит натрия, соединения типа NH 2 X. Все реакции присоединения идут быстро, в мягких условиях, однако образующиеся продукты, как правило, термодинамически не устойчивы. Поэтому реакции протекают обратимо, и содержание продуктов присоединения в равновесной смеси может быть низким.
Присоединение воды.
Альдегиды и кетоны присоединяют воду с образованием гидратов. Реакция протекает обратимо. Образующиеся гидраты термодинамически не стабильны. Равновесие смещено в сторону продуктов присоединения только в случае активных карбонильных соединений.

Продукт гидратации трихлоруксусного альдегида хлоральгидрат – устойчивое кристаллическое соединение, которое используется в медицине как успокаивающее и снотворное средство.
Присоединение спиртов и тиолов.
Альдегиды присоединяют спирты с образованием полуацеталей . При избытке спирта и в присутствии кислотного катализатора реакция идет дальше – до образования ацеталей

Реакция образования полуацеталя протекает как нуклеофильное присоединение и ускоряется в присутствии кислот или оснований.

Процесс образования ацеталя идет как нуклеофильное замещение ОН группы в полуацетале и возможен только в условиях кислотного катализа, когда группа ОН превращается в хорошую уходящую группу (H 2 O).

Образование ацеталей – обратимый процесс. В кислой среде полуацетали и ацетали легко гидролизуются. В щелочной среде гидролиз не идет. Реакции образования и гидролиза ацеталей играют важную роль в химии углеводов.
Кетоны в аналогичных условиях кеталей не дают.
Тиолы как более сильные нуклеофилы, чем спирты, образуют продукты присоединения и с альдегидами, и с кетонами.
Присоединение синильной кислоты
Синильная кислота присоединяется к карбонильным соединением в условиях основного катализа с образованием циангидринов.

Реакция имеет препаративное значение и используется в синтезе α-гидрокси- и α -аминокислот (см. лек. № 14). Плоды некоторых растений (например, горький миндаль) содержат циангидрины. Выделяющаяся при их расщеплении синильная кислота оказывает отравляющее действие.
Присоединение бисульфита натрия.
Альдегиды и метилкетоны присоединяют бисульфит натрия NaHSO 3 c образованием бисульфитных производных.

Бисульфитные производные карбонильных соединений – кристаллические вещества, не растворимые в избытке раствора бисульфита натрия. Реакция используется для выделения карбонильных соединений из смесей. Карбонильное соединение может быть легко регенерировано обработкой бисульфитного производного кислотой или щелочью:
Взаимодействие с соединениями общей формулы NH 2 X.
Реакции протекают по общей схеме как процесс присоединения-отщепления. Образующийся на первой стадии продукт присоединения не устойчив и легко отщепляет воду:

По приведенной схеме с карбонильными соединениями реагируют аммиак, первичные амины, гидразин, замещенные гидразины, гидроксиламин:

Образующиеся производные представляют собой кристаллические вещества, которые используют для выделения и идентификации карбонильных соединений.
2.2. Реакции по α -углеродному атому.
Кето-енольная таутомерия.
Водород в α -положении к карбонильной группе обладает кислотными свойствами, так как образующийся при его отщеплении анион стабилизируется за счет резонанса:

Результатом протонной подвижности атома водорода в α -положении является способность карбонильных соединений к образованию енольных форм за счет миграции протона из α -положения к атому кислорода карбонильной группы:

Кетон и енол являются таутомерами . Таутомеры – это изомеры, способные быстро и обратимо превращаться друг в друга за счет миграции какой-либо группы (в данном случае – протона). Равновесие между кетоном и енолом называют кето-енольной таутомерией.
Большинство карбонильных соединений существуют преимущественно в кетонной форме. Содержание енольной формы возрастает с увеличением кислотности карбонильного соединения, а также в случае дополнительной стабилизации енольной формы за счет водородной связи или за счет сопряжения.
Таблица 8. Содержание енольных форм и кислотность карбонильных соединений
Например, в 1,3-дикарбонильных соединениях подвижность протонов метиленовой группы резко увеличивается за счет электроноакцепторного влияния двух карбонильных групп. Кроме того, енольная форма стабилизируется за счет наличия в ней системы сопряженных α -связей и внутримолекулярной водородной связи:

Енолизация и образование енолят-анионов являются первыми стадиями реакций карбонильных соединений, протекающих по α -углеродному атому. Важнейшими из них являются галогенирование и альдольно-кротоновая конденсация .
Галогенирование
Альдегиды и кетоны легко вступают в реакцию с галогенами (Cl 2 , Br 2 , I 2) с образованием α –галогенпроизводных:

Реакция катализируется кислотами или основаниями. Скорость реакции не зависит от концентрации и природы галогена. Процесс протекает через образование енольной формы (медленная стадия), которая затем реагирует с галогеном (быстрая стадия). Таким образом, галоген не участвует в скорость-определяющей стадии процесса.

Если карбонильное соединение содержит несколько α -водородных атомов, то замещение каждого последующего происходит быстрее, чем предыдущего, вследствие увеличения их кислотности под действием электроноакцепторного влияния галогена. В щелочной среде ацетальдегид и метилкетоны дают тригалогенпроизводные, которые затем расщеплятся под действием избытка щелочи с образованием тригалогенметанов (галоформная реакция) :
Реакции конденсации
В присутствии каталитических количеств кислот или щелочей карбонильные соединения, содержащие α -водородные атомы, претерпевают конденсацию с образованием α-гидроксикарбонильных соединений.

В образовании связи С-С участвуют карбонильный атом углерода одной молекулы (карбонильной компоненты ) и α -углеродный атом другой молекулы (метиленовой компоненты ). Эта реакция носит название альдольной конденсации (по названию продукта конденсации ацетальдегида – альдоля).
При нагревании реакционной смеси продукт легко дегидратируется с образованием α,ß -непредельного карбонильного соединения:

Такой тип конденсации носит название кротоновой (по названию продукта конденсации ацетальдегида – кротонового альдегида).
В качестве метиленовой компоненты в реакциях конденсации могут выступать не только карбонильные соединения, но и другие С-Н-кислоты. Реакции конденсации имеют препаративное значение, так как позволяют наращивать цепь углеродных атомов. По типу альдольной конденсации и ретроальдольного распада (обратный процесс) протекают многие биохимические процессы: гликолиз, синтез лимонной кислоты в цикле Кребса, синтез нейраминовой кислоты.
Общая схема реакции:
Нуклеофил отдает субстрату свою пару электронов, за счет которой образуется новая связь, а галоген уходит со своей парой электронов в виде галогенид-аниона. При этом происходит алкилирование нуклеофила.
Для нуклеофильного замещения у атома углерода в состоянии sp 3 -гибридизации установлено два основных механизма: бимолекулярное нуклеофильное замещение (S N 2 ) и мономолекуляное нуклеофильное замещение (S N 1 ).
Бимолекулярное нуклеофильное замещение.
Бимолекулярное нуклеофильное замещение - это синхронный процесс, который протекает в одну стадию. Разрыв старой и образование новой связи происходят одновременно. Нуклеофил атакует субстрат со стороны, противоположной уходящей группе (с тыла), и постепенно вытесняет ее из молекулы:
Y: + R-Hal ® ® Y-R + Hal -
переходное
состояние
S N 2-реакции имеют следующие основные признаки.
- Кинетический признак
Скорость реакции зависит от концентрации и субстрата, и нуклеофила. Реакция имеет второй общий порядок (первый по субстрату и первый по нуклеофилу) и описывается кинетическим уравнением:
- v=k[Y]
- Стереохимический признак
Если нуклеофильное замещение происходит у асимметрического атома углерода, то имеет место обращение конфигурации, так как в переходном состоянии три нереагирующие группы и центральный атом углерода находятся в одной плоскости, а входящая и уходящая группы расположены на одной прямой, перпендикулярной этой плоскости. В результате структура выворачивается, как зонтик:
Мономолекуляное нуклеофильное замещение.
Мономолекулярное нуклеофильное замещение протекает в две стадии:
На первой стадии под действием растворителя происходит гетеролитический разрыв связи в субстрате, в результате чего образуется карбокатион. Процесс протекает медленно и определяет скорость реакции в целом. На второй стадии карбокатион быстро реагирует с нуклеофилом, давая продукт замещения.
Энергетическая диаграмма процесса имеет вид:
S N 1-реакции имеют следующие основные признаки.
- Кинетический признак
Скорость реакции зависит только от концентрации субстрата, поскольку нуклеофил не участвует в лимитирующей стадии процесса. Реакция имеет первый порядок и описывается кинетическим уравнением:
v=k
- Cтереохимический признак
Если нуклеофильное замещение происходит у асимметрического атома углерода, то, как правило, образуется рацемическая смесь, так как атака нуклеофилом плоского карбокатиона с обоих сторон равновероятна:
Факторы, влияющие на ход нуклеофильного замещения
Легкость протекания реакции и ее механизм зависят от многих факторов, среди которых можно выделить следующие:
- строение углеводородного радикала субстрата;
- природа уходящей группы;
- сила нуклеофила;
- природа растворителя.
Влияние строения углеводородного радикала.
Реакционная способность первичных, вторичных и третичных алкилгалогенидов в реакциях нуклеофильного замещения различна, причем порядок реакционной способности зависит от механизма реакции.
Скорость реакций, протекающих по механизму S N 1, зависит от стабильности карбокатиона, образующегося на первой стадии реакции. Таким образом, реакционная способность алкилгалогенидов в реакциях S N 1 возрастает в ряду:
который соответствует ряду стабильности карбокатионов:
Успех реакции S N 2 определяется эффективностью атаки нуклеофила на положительно заряженный реакционный центр субстрата. Поэтому электронодонорные радикалы R, понижая положительный заряд на реакционном центре, замедляет нуклеофильную атаку. В то же время увеличению объема R затрудняет подход нуклеофила к реакционному центру. Совместное действие индуктивного и объемного эффектов определяет ряд реакционных способностей субстратов в реакциях нуклеофильного замещения:
Высокой реакционной способностью независимо от механизма реакции обладают аллил- и бензилгалогениды. В процессе S N 1 они дают карбокатионы, стабилизированные засчет сопряжения:
Бензил-катион
Легкость, с которой аллил- и бензилгалогениды вступают в S N 2-реакции объясняют участием кратных связей в стабилизации переходного состояния.
Влияние природы уходящей группы.
Реакционная способность алкилгалоненидов зависит от прочности связи углерод - галоген, которая уменьшается в ряду:
C-F > C-Cl > C-Br > C-I.
Не менее важно, чтобы уходящая группа была термодинамически стабильна. (Она должна быть более устойчива, чем атакующий субстрат нуклеофил). Хорошими (относительно устойчивыми) уходящими группами являются слабые основания. Галогенид-анионы - хорошие уходящие группы. Их относительная стабильность возрастает по мере уменьшения их основности в ряду:
F - < Cl - < Br - < I -
Параллельно увеличивается и реакционная способность алкилгалогенидов независимо от того, по какому из двух механизмов протекает реакция:
RF < RCl < RBr < RI
Влияние природы нуклеофила.
Нулеофильность - это способность частицы взаимодействовать с атомом углерода, несущим целый или частичный положительный заряд. Нуклеофильность является кинетической характеристикой и определяется константами скоростей соответствующих реакций.
Нуклеофилы, как и основания, могут быть сильными и слабыми. Единой шкалы нуклеофильности не существует, так как относительная сила нуклеофила может изменяться в зависимости от природы субстрата и растворителя. Однако можно выделить следующие основные закономерности.
1) Отрицательно заряженные нуклеофилы сильнее, чем нейтральные молекулы (сопряженные им кислоты):
OH - > H 2 O; RO - > ROH; NH 2 - > NH 3
2) Для элементов одного периода с ростом электроотрицательности атома нуклеофильность уменьшается:
NH 2 - > OH - > F -
R 3 C - > RNH 2 - > RO - > F -
3) Электронодонорные заместители увеличивают, электроноакцепторные - уменьшают нуклеофильность. Например, для кислородсодержащих нуклеофилов установлен следующий ряд реакционной способности:
RO - > OH - > ArO - > RCOO -
В рассмотренных примерах порядок нуклеофильности реагентов совпадает с порядком их основности и объясняется теми же причинами. Однако сила нуклеофила определяется не только его основностью, но иполяризуемостью .
4) Для элементов одной подгруппы с возрастанием заряда ядра нуклеофильность увеличивается, несмотря на уменьшение основности:
RS --
I - - - -
Рост нуклеофильности связан с увеличением поляризуемости атомов и ионов по мере увеличения их радиуса. Чем выше поляризуемость нуклеофила, тем легче деформируется его электронное облако и тем в большей степени он способен передать электронную плотность на субстрат.
Такой порядок нуклеофильности может быть объяснен также с позиций принципа ЖМКО. Основность по Бренстеду проявляется во взаимодействии с жесткой кислотой Н + , в то время как нуклеофильность проявляется во взаимодействии с более мягким кислотным центром - атомом углерода, для которого предпочтительным будет взаимодействие с мягкими основаниями Льюиса - RS - и I - .
Кроме того, относительная сила нуклеофилов зависит от природы растворителя. Чем меньше размер аниона, тем лучше он сольватируется полярными протонными растворителями (т.е. растворителями, способными образовывать с анионом водородные связи), что снижает его реакционную способность. При замене растворителя порядок реакционной способности нуклеофилов может меняться на противоположный.
В соответствии с механизмами S N 2 и S N 1 природа нуклеофила оказывает влияние на ход S N 2-реакции, так как нуклеофил участвует в лимитирующей (и единственной) стадии процесса, и не влияет на скорость реакций, протекающих по механизму S N 1, лимитирующая стадия которых протекает без участия нуклеофила.
Влияние природы растворителя
Растворитель влияет на скорость и механизм реакций нуклеофильного замещения.
Протеканию реакции по механизму S N 1 способствуют сильноионизирующие растворители. К ним относятся полярные протонные растворители (вода, спирты, карбоновые кислоты), так как они хорошо сольватируют ионные интермедиаты: отрицательно заряженную уходящую группу - за счет водородных связей, карбокатион - за счет свободных пар электронов.
Влияние растворителя на S N 2-реакции проявляется в меньшей степени и зависит от распределения зарядов в исходном и переходном состояниях. Как правило, их скорость уменьшается с ростом полярности растворителя и увеличивается при переходе от протонных растворителей к апротонным (диметилформамид, диметилсульфоксид, ацетонитрил). В апротонных растворителях, которые не способны к образованию водородных связей, нуклеофил (а это, как правило, анион) в меньшей степени сольватирован и, следовательно, обладает большей силой, что важно для S N 2-реакции.
Таким образом, протеканию реакций по механизму S N 2 способствуют:
- субстрат с углеводородным радикалом малого объема (первичным);
- апротонный растворитель;
- сильный нуклеофил.
Реализации механизма S N 1 способствуют:
- субстрат с углеводородным радикалом разветвленного строения (третичным);
- полярный протонный растворитель;
- слабый нуклеофил.
По легкости замещения галогена независимо от механизма реакции галогенпроизводные располагаются в следующий ряд:
аллил- и бензилгалогениды > алкилгалогениды > винил- и арилгалогениды
Галогенпроизводные, содержащие связь (винил- и арилгалогениды), обладают очень низкой реакционной способностью. Реакция протекает по иному механизму. Малую подвижность галогена в винил- и арилгалогенидах объясняют увеличением прочности связи C-Hal за счет сопряжения пары электронов галогена с электронами p -связей:
Примеры реакций нуклеофильного замещения
Реакции нуклеофильного замещения галогена широко используются в органическом синтезе. С их помощью можно заменять галоген на другие функциональные группы или углеводородные радикалы и получать из галогенпроизводных любые классы органических соединений.
Примеры синтетического использования галогенпроизводных алифатических углеводородов приведены в таблице.
Таблица 7. S N -реакции галогенпроизводных
| Субстрат | + | нуклефил | ® | продукт + уходящая группа |
| Получение спиртов | ||||
| R-Hal | + | OH - (H 2 O) | ® | R-OH + Hal - (HHal) |
| CH 3 Br | + | NaOH | CH 3 OH + NaBr | |
| (CH 3) 3 CCl | + | H 2 O | ® | (CH 3) 3 COH + HCl |
| CH 2 =CH-CH 2 Cl | + | H 2 O | ® | CH 2 =CHCH 2 OH+HCl |
| Получение простых эфиров | ||||
| R-Hal | + | R / O - | ® | R-OR / + Hal - |
| СH 3 I | + | CH 3 CH 2 O - Na + | ® | CH 3 OCH 2 CH 3 + NaI |
| Получение сложных эфиров | ||||
| R-Hal | + | R / COO - | ® | R / COOR + Hal - |
| CH 3 CH 2 I | + | CH 3 COO - Na + | ® | CH 3 COOCH 2 CH 3 + NaI |
| Получение тиолов | ||||
| R-Hal | + | SH - | ® | R-SH + Hal - |
| CH 3 СH 2 Br | + | NaHS | ® | CH 3 СH 2 SH + NaBr |
| Получение сульфидов | ||||
| R-Hal | + | R / S - | ® | R-SR / + Hal - |
| CH 3 СH 2 Br | CH 3 СH 2 S - Na + | ® | (CH 3 СH 2) 2 S + NaBr | |
| Получение аминов и аммониевых солей | ||||
| R-Hal | + | NH 2 - | ® | RNH 2 + Hal - |
| R-Hal | + | R / 3 N | ® | R R / 3 N + Hal - |
| Получение нитрилов | ||||
| R-Hal | + | Сє N - | ® | R- Сє N + Hal - (S N 2) |
| CH 3 СH 2 Br | + | NaCN | ® | CH 3 СH 2 CN + NaBr |
| Получение нитросоединений | ||||
| R-Hal | NO 2 - | ® | R-NO 2 + Hal - (S N 2) | |
| CH 3 CH 2 I | AgNO 2 | ® | CH 3 CH 2 NO 2 + AgI | |
| Получение галогенпроизводных | ||||
| R-Hal | + | I - | ® | R-I + Hal - (S N 2) |
| CH 3 Cl | + | NaI | ® | СH 3 I + NaCl |
Винил- и арилгалогениды инертны по отношению к нуклеофильным реагентам. Замещения галогена в галогенбензолах возможно только в очень жестких условиях, например:
Введение электроноакцепторных заместителей в орто - и пара -положения к галогену активизируют галогенарены в S N -реакциях:
Аналогично 2,4-динитрофторбензол взаимодействует с аминогруппами аминокислот и пептидов, что используется для установления их аминокислотного состава:
В случае вторичных и первичных алкилгалогенидов, как правило, реакция идёт как бимолекулярное нуклеофильное замещение S N 2 :
S N 2 реакции являются синхронными процессами – нуклеофил (в данном случае OH -) атакует атом углерода, постепенно образуя с ним связь; одновременно с этим постепенно разрывается связь С-Br. Уходящий из молекулы субстрата бромид-ион в называется уходящей группой или нуклеофугом .
В случае S N 2 реакций скорость реакции зависит от концентрации и нуклеофила, и субстрата:
v = k [S]
v – скорость реакции,
k- константа скорости реакции
[S] – концентрация субстрата (т.е. в данном случае алкилгалогенида)
– концентрация нуклеофила
В случае третичных алкилгалогенидов нуклеофильное замещение идёт по механизму мономолекулярного нуклеофильного замещения S N 1 :

трет-бутилхлорид трет-бутанол
Механизм этой реакции очень напоминает механизм реакций обмена в неорганической химии, является диссоциативным и идёт в две стадии:

карбокатион нуклеофил продукт
В случае S N 1 реакций скорость реакции зависит от концентрации субстрата и не зависит от концентрации нуклеофила: v = k [S]
По таким же механизмам идут реакции нуклеофильного замещения и в случае спиртов и во многих других случаях.
Кроме реакций S N 1 и S N 2 замещение может идти по механизму S N i . Нуклеофильное замещение у винильного атома углерода может осуществляться по 10 различным механизмам, а нуклеофильное замещение в ароматических системах может идти по 4 различным механизмам.
Реакции элиминирования (отщепления) – дегидрогалогенирования
В результате реакций элиминирования в случае алкилгалогенидов образуется алкены и галогеноводороды.
Например, при нагревании этилхлорида с щёлочью в спирте происходит элиминирование HCl и идёт образование этилена:

Следует обратить внимание на то, что если проводить эту реакцию в воде, а не в спирте, то основным продуктом будет спирт, а не алкен.
В случае несимметричных алкилгалогенидов реакции дегидрогалогенирования идут в соответствии с правилом Зайцева :
Отщепление атома водорода в реакциях отщепления HX происходит от наименее гидрогенизированного атома углерода.
Например, отщепление бромоводорода от 2-бромбутана может происходить двумя путями:

Действительно, реализуются оба пути, но преимущественно образуется бутен-2 (80%), в то время как бутен-1 образуется в малом количестве (20%).
Механизмы реакций элиминирования
Элиминирование галогеноводородов может осуществляться по 3 основным механизмам: E1, E2 и E1cb
Механизм E1
Алкилгалогенид диссоциирует с образованием карбокатиона и галогенид-иона. Основание (B:) отрывает от образующегося карбокатиона протон с образованием продукта – алкена:

субстрат карбокатион продукт
Такой механизм характерен для третичных алкилгалогенидов.
Механизм E1cb
В этом случае последовательность другая: основание отрывает от алкилгалогенида протон с образованием карбоаниона, от которого потом отщепляется галогенид-ион с образованием алкена:

карбоанион
Этот механизм встречается нечасто, например он показан для реакции элиминирования HF от 1,1,1-трифтор-2,2-дихлорэтана.
Механизм E2
В этом случае отрыв протона и галогенид-иона происходит синхронно, т. е. одновременно:

Механизм E2 характерен в основном для первичных и вторичных алкилгалогенидов.
Аналогичные механизмы наблюдаются в случае элиминирования воды от спиртов и в других случаях.